アドバンテームの危険性と安全性評価【人工甘味料・食品添加物】

アドバンテームは、発がん性なし、変異原性なし、毒性なしとの研究結果が報告されていますが、ショ糖(スクロース)の20000倍の甘さがあるため、大量摂取は甘すぎて受け入れられず、1日の安全許容量は0~5mg/kg体重です。腸管から吸収されず、カロリーもなく、虫歯にもなりにくい甘味料です。
アドバンテームの化学的性質と詳細
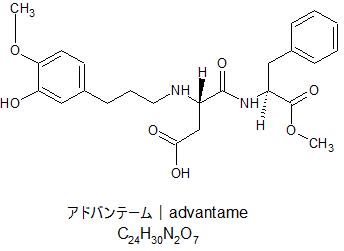
アドバンテーム(Advantame|IUPAC:Methyl N-[3-(3-Hydroxy-4-methoxyphenyl)propyl]-L-α-aspartyl
-L-phenylalaninate monohydrate)は、化学式C24H30N2O7、化学式量(FW:formula weight)476.52(C24H30N2O7・H2Oの場合)、水には難溶の人工甘味料です。
アドバンテームの甘さは、ショ糖の20000倍~30000倍で、味の素が生み出した「アミノ酸系高甘味度甘味料」で、欧州委員会からは2014年5月15日、アメリカのFDAからは2014年5月21日に認可を受けています。アドバンテームは胃腸管からほとんど吸収されません。
カロリーはほぼゼロ、腸管からも吸収されない、甘さはショ糖(スクロース)の20000倍と、極微量で同等の甘さが出る甘味料です。
アドバンテームの危険性評価
アドバンテームの濃度50,000ppmから8447mg/kg体重/日のえさを、2世代のラットに与えた実験では、死亡率、体重、生殖機能、遺伝毒性、変異原性などの影響は認められなかったとされています。
Mean advantame intakes from each of the diets were 164, 833, and 4410 mg/kg bw/day among F0 males, and 204, 1036, and 5431 mg/kg bw/day among F1 males. F0 and F1 females had comparable intakes up to lactation, when intakes increased (up to 8447 mg/kg bw/day from 50,000 ppm diet). No treatment-related effects on mortality, body weights, reproduction, litter observations, or postnatal offspring development were noted.
No treatment-related effects on mortality, body weights, reproduction, litter parameters, or postnatal offspring development.
引用元:https://www.sciencedirect.com/science/article/abs/pii/S0278691511003243
アドバンテーム微量摂取では発がん性はない(ラットに対する高用量試験)
A high incidence of a pale and swollen anus and changes in fecal composition were observed in the high-dose groups. There was no effect of treatment on mortality.
引用元:https://www.sciencedirect.com/science/article/abs/pii/S0278691511002845
また、別の実験において、ラットのオス・メスそれぞれ55匹に、アドバンテーム(純度98.9〜99.8%)を0ppm、2000ppm、10,000ppm、50,000ppmの濃度で104週間(約26ヶ月)投与した実験において、アドバンテーム濃度が高かったグループは肛門に青白い腫れ、糞便組成の変化があったとのことですが、発がん性はなかったとされています。
上記の2つの実験では、アドバンテーム濃度が50,000ppm未満においては毒性は見受けられないとされていて、50,000ppmがアドバンテームの安全濃度ではないかと言われています。
アドバンテームの人体治験でも異常はなし
48名に対して0.1mg/kg体重、0.25mg/kg体重、0.5mg/kg体重と濃度を変えつつ摂取させるものと、プラセボ群を用意した治験が行われています。
Advantame, a new, high-intensity sweetener that is thought not to be absorbed from the human gastrointestinal tract in appreciable quantities, was evaluated for safety and tolerability in a total of 48 healthy adult volunteers in 2 studies. In the first study 24 subjects were randomized to receive escalating single doses of 0.1, 0.25, or 0.5 mg/kg of body weight, and pharmacokinetic and safety parameters were assessed subsequently for 8 days.
引用元:https://www.sciencedirect.com/science/article/abs/pii/S0278691511002870
これらの治験群に対して、バイタルサイン、心電図、身体検査において、臨床的変化はなかったと報告されています。またアドバンテーム摂取後の血漿中濃度も、化学的に定量できないほどに低いと報告されています。血液中のアドバンテームは、測定する事ができないほどに少ないか、アドバンテームが血液中に溶け出していないと考えられます。
アドバンテームの安全摂取量は0~5mg/kg体重/日
JECFA(FAO/WHO食品添加物専門家会議)において、アドバンテームの安全許容量(ADI)は1日あたり0~5mg/kg体重とされています。最大濃度で、体重50kgの人で計算すると
5mg/kg × 50kg = 250mg
250mg = 0.25g
となります。体重50kgの人が、1日に摂取しても安全だと考えられるアドバンテーム量は0.25gであるということになります。
アドバンテーム0.25gと同じ甘さをショ糖(スクロース)で再現するには、この20000倍の量を用意する必要があり
0.25g × 20000 = 5000g
5000g = 5kg
となります。これで分かる通り、同じ甘さをショ糖(スクロース)で再現する方が危険です。
アドバンテームの安全性評価
これらの情報を元に、人体実験(引用元の治験)で試された最大容量0.5mg/kgを分かりやすくすると、体重50kgの大人の人の場合は、
0.5 × 50 = 25mg
となります。アドバンテームは、低く見積もってもショ糖(スクロース)の20000倍の甘さがあるため、アドバンテーム25mgと同じ甘さを再現するためには、
25mg × 20000 = 500,000mg
500,000mg = 500g
となり、500gのショ糖を必要とします。この場合、ショ糖のカロリーは1gあたり約4kcalなので、500gのショ糖のカロリーは2000kcalとなります。
常識的に考えて、ショ糖500gを毎日摂取すると虫歯にもなりやすく、明らかに過剰摂取で、同じ甘さを出すためにショ糖を使用する方が危険です。
アドバンテームの場合は、発がん性なし、虫歯にならない、カロリーほぼなし、毒性なし、腸管から吸収されない、バイタルサイン異常なしなど、陰謀論者(偽医者等)が言うような危険性や毒性は科学的には証明できず、同じ甘さを得るためにたったの25mgのみで済むため、デメリットはほとんどありません。
むしろ、そこまで甘くする必要はないと思われるので、アドバンテームを使用する必要もないと考えられます。少量の食品添加物で十分な甘さを出せるのは科学の進歩ではありますが、甘さだけ増やしても栄養摂取効率が落ちるのではあまり意味がなく、総合栄養食(レーション)などでは活かせそうですが、一般向けでどこまで生かせるかは未知数です。
アドバンテームは、甘味は感じるが、栄養にならない上に、排泄をしなければならないため、エネルギーを無駄に消耗します。アドバンテームを含む飲料をいくら摂取しても、健康面で向上は期待できませんので、通常の栄養バランスを考えた食事を取る必要があります。
出典・参考
Acute and multiple-dose studies to determine the safety, tolerability, and pharmacokinetic profile of advantame in healthy volunteers
https://www.sciencedirect.com/science/article/abs/pii/S0278691511002870
Chronic toxicity and carcinogenicity of N-[N-[3-(3-hydroxy-4-methoxyphenyl) propyl]-α-aspartyl]-l-phenylalanine 1-methyl ester, monohydrate (advantame) in the rat
https://www.sciencedirect.com/science/article/abs/pii/S0278691511002845
A two-generation reproductive toxicity study of the high-intensity sweetener advantame in CD rats
https://www.sciencedirect.com/science/article/abs/pii/S0278691511003243
Advantame – An overview of the toxicity data
https://www.sciencedirect.com/science/article/abs/pii/S0278691511002900
Advantame
https://www.taylorfrancis.com/chapters/edit/10.1201/b11242-6/advantame-ihab-bishay-robert-bursey
Acute and multiple-dose studies to determine the safety, tolerability, and pharmacokinetic profile of advantame in healthy volunteers
https://www.sciencedirect.com/science/article/abs/pii/S0278691511002870
アドバンテーム|FUJIFILM
https://labchem-wako.fujifilm.com/jp/product/detail/W01W0101-2680.html
アドバンタム|Chemical Book
https://www.chemicalbook.com/ChemicalProductProperty_JP_CB22709499.htm
(案)添加物評価書|アドバンテーム|2013年5月
https://www.fsc.go.jp/iken-bosyu/pc1_tenkabutu_advan_250528.pdf
アドバンテームの食品添加物の指定に関する部会報告書(案) 資料1-2|厚生労働省
https://www.mhlw.go.jp/file/05-Shingikai-11121000-Iyakushokuhinkyoku-Soumuka/0000028243.pdf
アドバンテームの食品添加物の指定に関する部会報告書(案)資料4|厚生労働省
https://www.mhlw.go.jp/file/05-Shingikai-11121000-Iyakushokuhinkyoku-Soumuka/0000030813.pdf
味の素(株)の新甘味料「アドバンテーム」欧州と米国で食品添加物認可を取得
https://www.ajinomoto.co.jp/company/jp/presscenter/press/detail/2014_05_27.html
指定添加物リスト|公益財団法人 日本食品化学研究振興財団 事務局
https://www.ffcr.or.jp/tenka/list/post-11.html
各添加物の使用基準及び保存基準|公益財団法人 日本食品化学研究振興財団 事務局
https://www.ffcr.or.jp/webupload/74a51493d997785a77ea40142cf05a79c6b52db7.pdf
食品添加物|厚生労働省
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/shokuhin/syokuten/index.html
第二世代の糖アルコール
https://www.bfsci.co.jp/pdf/catalogue/03.pdf