ALC-0159とは【2-[(ポリエチレングリコール)-2000]-N,N-ジテトラデシルアセトアミド】添加物解説
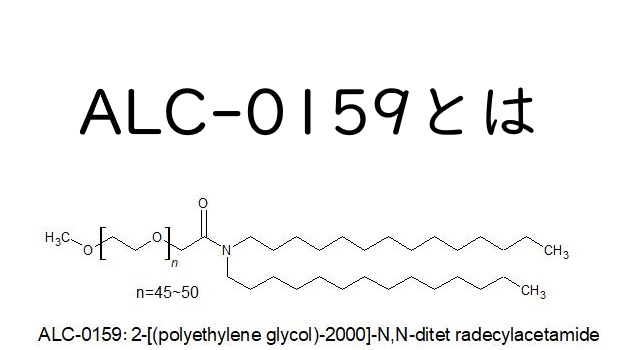
ここでは、ALC-0159:2-[(ポリエチレングリコール)-2000]-N,N-ジテトラデシルアセトアミド単体の構造や化学式などの性質について解説しています。特例承認医薬品「コミナティ」に含まれている添加物で、筋肉注射に使われているものです。
[su_box title="注記" style="glass" box_color="#fffac9″ title_color="#323232″ radius="10″]
- 本ページは、添加物に関連する行為を推奨、否定するものでもありません。
- 公的機関や開発元とは一切の利害関係がありません。
- 特定の立場・意見を持つ人への如何なる侵害を示唆するものではありません。
- 化学的構造については公表されている範囲でのみまとめており、正確性を完全には保証しません。
[/su_box]
概要「ALC-0159:2-[(ポリエチレングリコール)-2000]-N,N-ジテトラデシルアセトアミド」
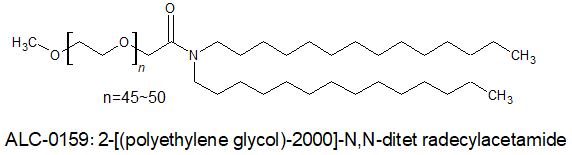
ALC-0159(2-[(polyethyleneglycol)-2000]-N,N-ditetradecylacetamide)は、分子式C31H63NO2・[C2H4O]n、分子量481.83+[44.05]nの高分子で、Phizerのワクチンに含まれている添加物、ワクチンのmRNAを包んでカプセル化するために必要な成分の1つです。
From all the excipients officially declared one with the ability to cause allergic reactions is ALC-0159 since it contains polyethylene glycol (PEG) or macrogol.
出典:https://onlinelibrary.wiley.com/doi/full/10.1111/all.14711
PEGとマクロゴールを含むことから、アレルギー反応を起こすのは、ALC-0159である可能性があるとの記述がありました。この根拠は以下の画像のとおりで、
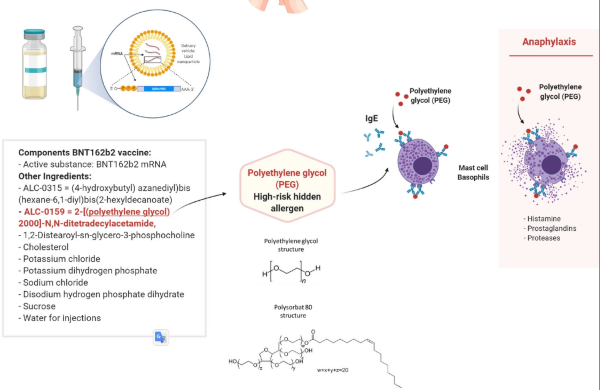
物質内にポリエチレングリコール(polyethylene glycol)を含んでいることから、警戒されているとのことです。PEG(polyethylene glycol)は多く使用されていますが、特定の条件がそろうとアレルギー反応を起こす場合があるため、安易に安全であるとはいい切れません。
別の出典より、アジアの一部の症例で、甲状腺に問題があった方が、ワクチン接種後に、バセドウ病を発症した例があるそうですが、ケースが少なすぎて断定できる情報は不十分でした。念のため、甲状腺に関する持病がある方もALC-0159を含むワクチン接種は控えておいたほうが良いかもしれませんが、かかりつけ医にまず相談してから決断してください。
ALC-0159の危険性・安全性・毒性
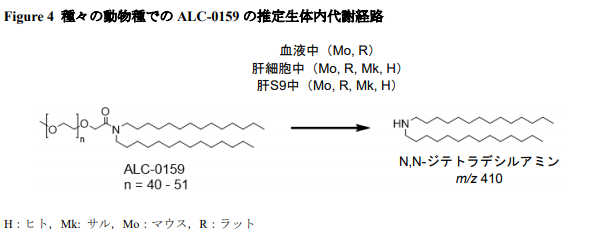
ALC-0315、および、ALC-0159は血中から肝臓にすみやかに分布することが示された。また、ALC-0315、および、ALC-0159はそれぞれ投与量の約1%および約50%が未変化体として糞中に排泄され、尿中においてはいずれも検出限界未満であった。
血中のALC-0315、および、ALC-0159 は、投与後24時間までにすみやかに肝臓へ分布した。また、投与後24時間の血漿中濃度は最高血漿中濃度の1%未満であった。見かけの終末相消失半減期(t½)は血漿中および肝臓中で同程度で、ALC-0315は6~8日、ALC-0159は2~3日であった。
出典:https://www.pmda.go.jp/drugs/2021/P20210212001/672212000_30300AMX00231_I100_1.pdf
ALC-0159はALC-0315と同様に、肝臓で代謝されて、糞尿として排泄されるとのことです。肝臓を経由して代謝されるため、ワクチン接種後には肝臓に負担がかかる行動(飲酒・喫煙等)は避けるのがよいと、公表されています。
PEGアレルギーがあった人は要注意
Although the trigger of the adverse allergic reactions suffered by the two NHS workers after receiving the vaccine BNT162b2 against COVID-19 has yet to be determined, the potential role of the excipient ALC-0159 containing PEG as a high-risk hidden trigger of dangerous allergic reactions should be carefully considered before advising the administration of BNT162b2 vaccine. However, if hypersensitivity reactions to PEG and PEG analogous will be ruled out as a reason for the anaphylactic reactions observed, not all patients with food and drug allergies would have to be advised against BNT162b2 vaccination, but just those allergic to PEG, PEG analogues, or other excipients.
出典:https://onlinelibrary.wiley.com/doi/full/10.1111/all.14711
食物アレルギーまで気にする必要はないですが、PEG(polyethylene glycol)摂取に伴うアレルギー反応、アナフィラキシー反応があった経験がある方は、このALC-0159を含むワクチンを摂取する時に、担当医や現場の医師、かかりつけ医の診断があった方がよいでしょう、とのことです。ただし、実験結果などが記載されていたわけではないので、注意喚起の領域を出ません。
PEG(polyethylene glycol)アレルギーに関しての注意喚起はひとつではなく、複数提起されています。ポリエチレングリコール(PEG|polyethylene glycol)によるアレルギーが、まずひとつ、今回のワクチンで心配されている要素なのは確実で、PEG(polyethylene glycol)でアレルギー反応が出る事実も確認されています。心配な方は摂取前の診断などで、確認しておきましょう。
参考:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8023205/
ワクチン接種の有効性とリスク
ワクチン接種に伴う副反応ではなく、ワクチン接種を受けないほうがいい人、受けられない人の条件に触れておきます。
【Vaccination unproblematic from the current allergological point of view】
– Allergic asthma
– Allergic rhinoconjunctivits
– Atopc eczema
– Food allergy
– Insect venom allergy
– Allergic contact eczema
– Urticaria
– History of drug eruption
– Delayed local reactions to vaccinations【Vaccination with increased risk awareness* or preceding allergic workup】
Anaphylaxis treated by a physician
– during a vaccination or medical procedure like coloscopy, surgical intervention under general anesthesia
– after (repeated) drug intake
– of unclear pathogenesis【No vaccination according to summary of product characteristics and from an allergological point of view】
History of severe allergic reactions to one or several of the vaccine ingredients
【おそらく接種に問題がない症状・持病等】
- アレルギー性喘息
- アレルギー性鼻結膜
- アトプセ湿疹
- 食物アレルギー
- 昆虫毒アレルギー
- アレルギー性接触湿疹
- 蕁麻疹
- 薬物発疹の病歴
- ワクチン接種に対する局所反応の遅延
【慎重なワクチン接種、または、先にアレルギーの精密検査必要】
- 医師によって治療されたアナフィラキシー
- ワクチン接種中または結腸鏡検査などの医療処置中
- 全身麻酔下での外科的介入
- (反復)薬物摂取後
- 病因が不明
【接種を推奨しない】
- 1つまたは複数のワクチン成分に対する重度のアレルギー反応の病歴
過去、ワクチンを摂取して重度のアレルギー反応があった方は、ワクチンの接種は避けたほうがよく、かかりつけ医への相談が必須です。また、
- アナフィラキシーショック経験者
- 投薬治療中
- 全身麻酔を伴う外科手術経験者
などの方は、慎重にワクチン接種をしなければいけないとの記載があります。ここで、詳細を語ることは不適切かと思われるため、ワクチン接種前の医師の判断、及び、各自の治療歴などをケースバイケースで判定して、接種するか、接種しない(できない)か検討してください。
出典・参考
COMIRNATY intramuscular injection
https://www.med.or.jp/dl-med/kansen/novel_corona/sokuho/comirnaty.pdf
厚生労働省|新型コロナワクチンの副反応に係る体制の概要について
【参考:添加物ALC-0315及びALC-0159の安全性について 】
○ ALC-0315及びALC-0159は添加剤としての使用前例がなく、DSPCは特定の製剤又は特定の条件下においてのみ使用が認められている添加物であるが、本剤の製剤特性を担保するために必要。
○ 製剤を用いた毒性試験のうち、ラットにおける反復筋肉内投与毒性試験では、肝臓への影響(血中GGTの増加及び肝細胞の空胞化)が認められたが、毒性学的意義は低いと考えられた。
→これらの添加剤を使用することは可能であるが、長期間の反復投与毒性が評価されていないことから、これらの添加剤は、本剤の用法・用量に限った使用とすべきであると判断された。
https://www.mhlw.go.jp/content/10601000/000738916.pdf
SARS-CoV-2 mRNA Vaccine (BNT162, PF-07302048)2.6.6 毒性試験の概要文
https://www.pmda.go.jp/drugs/2021/P20210212001/672212000_30300AMX00231_J100_1.pdf
Allergic reactions to the first COVID-19 vaccine: A potential role of polyethylene glycol?
https://onlinelibrary.wiley.com/doi/full/10.1111/all.14711
Anaphylactic reactions to mRNA COVID-19 vaccines: A call for further study
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8023205/
Two Cases of Graves’ Disease Following SARS-CoV-2 Vaccination: An Autoimmune/Inflammatory Syndrome Induced by Adjuvants